كيف استطاعت الكيمياء السيطرة علينا؟ الجزء الثاني
كيف تعمل الأشياء ؟

لقد تناولنا في الجزء الأول التفسيرات الكيميائية لبعض الممارسات الحياتية التي نقوم بها دائمًا ووعدناكم بأن نلقاكم في الجزء الثاني من المقال…
كيمياء لون ورائحة الطعام المطهو
أتذكر في أيام العطل عندما كنت تخرج مع أصدقائك وتقررون أن تتناولوا في إحدى المطاعم فتمرون على المطاعم واحدًا تلو الآخر فتقول أنت: “يبدو أن هذا المطعم يطبخ طعامًا لذيذًا”، فيرد أحد أصدقائك: “لا هناك مطعم تفوح منه رائحة أزكى”، إذن ما هو الشيء الذي جعلكم تختارون مطعمًا دون الآخر؟ الرائحة.. لكن كيف تتكون الرائحة؟ وما هي الرائحة؟
حسنًا لنبسط الأمور ولنختر رائحة الدجاج المشوي، إنها رائحة لذيذة جدًا ويحبها الكثير من الناس، يحصل تفاعل كيميائي أثناء طهي الدجاجة وهو تفاعل يسمى تفاعل مايلارد (Maillard reaction)، التفاعل يحصل بين السكر والأحماض الأمينية الموجودة في الدجاج ليكوّن مركب الـglycosylamine، كما في المعادلة أدناه، يعيد مركب الـglycosylamine ترتيب ذراته مرارًا و تكرارًا، ويتفاعل مع مواد أخرى ليكون روائح وألوان وأطعمة مختلفة للطعام المطبوخ، لا يقتصر تفاعل مايلارد على الدجاج المشوي فقط وإنما أيضًا على اللحم المشوي ورائحة وطعم الخبز، اللون البني المقرمش لخبز التوست أيضًا يخضع لتفاعل مايلارد.

تفاعل السكر مع الأحماض الأمينية لتشكيل مركب Glycosylamine
إعلان

يتغير ترتيب ذرات مركب glycosylamine باستمرار ويتشكل ليتفاعل مع مواد أخرى تحت ظروف حمضية أو قاعدية
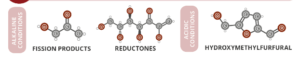
تفاعل مركب glycosylamine مع مركبات ثانية تحت ظروف قاعدية، ينتج مركبات مختلفة عن التي تنتج تحت ظروف حمضية، لذلك تؤثر إضافة الليمون والخل وبيكربونات الصودا على طعم ولون الطعام المطبوخ، فكل مركب من هذه المركبات له رائحة ولون وطعم خاص يختلف عن الآخر [8]، الصورة أدناه توضح لون وطعم ورائحة كل مركب ينتج عن التفاعل:
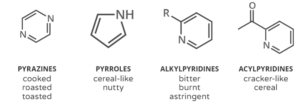

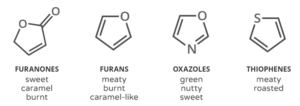

كيمياء النظارات الشمسية
يقترب الصيف، يبدأ الناس باختيار نظاراتهم الشمسية المفضلة، لكن سنتعرف كيف يمكن للكيمياء مساعدة النظارات الشمسية في حماية أعيننا وما المواد المصنوعة منها.
عادة تصنع عدسات النظارات الشمسية إما من الزجاج أو البلاستيك مثل متعددات الكربون polycarbonate
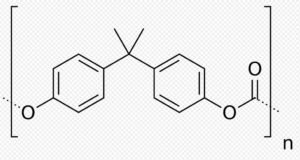
أو مركب PADC

كما أن استخدام الألمنيوم والفضة للعدسات يعطي تأثيرًا كالمرآة، أما أكاسيد السيليكون والمعادن SiO ، TiO ،Fe2O3 ،MnO2 تستخدم لتقليل امتصاص الأشعة فوق البنفسجية الصادرة عن الشمس.
بالنسبة للعدسات اللونية (التي تتغير لونها مع تعرضها للشمس)، فهي تُصنع من مواد عضوية أو غير عضوية.
العدسات اللونية التي تصنع من مواد غير عضوية وعادة ما تكون العدسات زجاجية مثل أملاح هاليدات الفضة (AgCl) التي تتفاعل مع الأشعة فوق البنفسجية لتكون عنصر الفضة مسببة اسوداد العدسات. أنظر للتفاعل التالي:
AgCl —– UV light —-> Ag + Cl
تفاعل مركب كلوريد الفضة مع الأشعة فوق البنفسجية لتكوين عنصر الفضة والكلور، وعنصر الفضة يسبب تغييرًا في لون العدسات للون الأسود.
أما عند استخدام مركبات عضوية وهي التي تتكون منها العدسات البلاستيكية، فإن بعض حلقات مركب الـNaphthopyran تفتح وتغير من شكلها عند التعرض للأشعة فوق البنفسجية مما يسبب تغير لون المركب فيعطي لونًا أسودًا [9].
يتفاعل مركب الـNaphthopyran مع الأشعة فوق البنفسجية مما ينتج عنه فتح لبعض حلقات المركب فيتحول لون المركب من شفاف إلى أسود
كيمياء كريمات واقيات الشمس
تأتي شمس الصيف مع مخاطر عديدة نتيجة التعرض لها بسبب ارتفاع حرارتها الشديد، لذا يقوم العديد منا بوضع الواقيات الشمسية لكن ما الكيمياء وراء الواقيات سنتعرف عليها الآن.
بدايةً سنتعرف على أنواع الإشعاعات فوق البنفسجية الصادرة عن الشمس:

الأشعة من نوع UVA ذات طول موجي يتراوح من 320 – 400 نانوميتر التي تمثل حوالي 95% من الإشعاعات فوق البنفسجية الصادرة عن الشمس والتي تصل لسطح الأرض تعبُر عميقًا في الجلد وتسبب السرطانات منها سرطان الجلد.

الأشعة من نوع UVB ذات طول موجي يتراوح من 290 – 320 نانوميتر تمثل حوالي 5% من الإشعاعات فوق البنفسجية الصادرة عن الشمس والتي تصل لسطح الأرض وتسبب ضررًا مباشرًا لـ DNA الخلية وتسبب سرطانات منها سرطان الجلد.

الأشعة من نوع UVC ذات طول موجي يتراوح من 290 – 100 نانوميتر، عادة ما تقوم طبقة الأوزون بالتخلص من هذه الإشعاعات ولا تصل لسطح الأرض ولا تسبب أي أضرار.
التركيب الكيميائي للواقيات الشمسية تتكون إما من مواد غير عضوية مثل أكسيد الزنك وأكسيد التيتانيوم اللذان يمتصان الأشعة فوق البنفسجية الصادرة عن الشمس.
أو مكونات عضوية ولها أنواع مختلفة اعتمادًا على نوع الموجة التي يمتصها المركب العضوي.
يذكر هذا الجدول المواد الكيميائية المختلفة التي تمتص الأشعة فوق البنفسجية [10]، حيث إن كل مركب مختص بامتصاص طول موجي معين للأشعة فوق البنفسجية:

UVA & UVB Blockers: المركبات التي تمتص الأشعة فوق البنفسجية من نوع ب و أ
UVB Blockers: المركبات التي تمتص الأشعة فوق البنفسجية من نوع ب
UVA Blockers: المركبات التي تمتص الأشعة فوق البنفسجية من نوع أ
كيمياء الألعاب النارية
تنطلق الألعاب النارية ذات الألوان العديدة والأصوات المتنوعة مما يثير انتباه الناس عند انطلاقها، لكن حتى الكيمياء لها علاقة كبيرة بتلك الألوان والأصوات سنتعرف عليها.

الالعاب النارية المنفجرة التي تستخدم عادة في أعياد رأس السنة:

يتكون الانفجار بسبب خليط من المواد الكيميائية وهي عبارة عن مادة مؤكسدة مع الكبريت والألمنيوم، حيث يعطي انفجار هذا الخليط ضوء قويًا مصحوبًا بصوت مرتفع، يضاف أحيانا بارود الأسلحة النارية لزيادة صوت الإنفجار .
الألعاب النارية ذات أصوات الخشخشة مثل المفرقعات الصغيرة التي يتم اشتعالها ورميها على الأرض فتعطي صوتًا مفرقعًا، تتكون هذه المفرقعات من رباعي أكسيد الرصاص مع خليط من الألمنيوم والماغنيسيوم، ولكن بسبب سُمّية عنصر الرصاص، فإن عنصر البيزموث Bismuth هو المستخدم حاليًا في هذه المفرقعات.

المركبات الموجودة في الألعاب النارية التي تعطي صوت خشخشة (ألعاب نارية مفرقعة).

أما الألعاب النارية التي تعطي صوتًا كالصفير فيدخل في تركيبها مركبات عضوية حلقية مثل المواد الموضحة لدينا بالصورة:

تخلط هذه المواد مع مواد مؤكسدة وتحزم جيدًا في أنبوب صغير وعند حدوث انفجار صغير تحرر المركبات العضوية الحلقية غازاتٍ نتيجة لاحتراق المزيج، مما يؤدي لإنشاء موجات تتدفق ضمن الأنبوب فيعطي صوت الصفير [11].

كيمياء الألوان
عدد كبير من المركبات غير العضوية تستخدم ضمن الطلاء لإعطاء صبغة لونية له وذلك بسبب أن تلك المركبات تمتص الأشعة الضوئية وتطلق موجة معينة دون أن تمتصها وبذلك نرى الصباغ بهذا اللون:
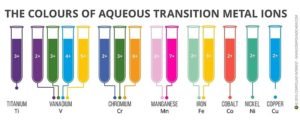
توضح الصورة المكون غير العضوي لكل لون مختلف من الطلاء:

الذي لا يعلمه الكثير منا أن المعادن لها ألوان مختلفة وكل معدن يتميز بلون خاص به، وليس لونًا واحدًا فقط وإنما عدة ألوان، الكثير من المعادن والمركبات يتغير لونها اعتمادًا على درجة التأكسد المتواجدة فيها، فمثلًا، لعنصر الكروم 3 ألوان مختلفة أثناء وجوده في درجات أكسدة مختلفة، Cr+2 لونه أزرق، بينما Cr+3 لونه أخضر، بينما Cr+6 لونه برتقالي، وهكذا لباقي العناصر، وبالتالي وضع هذه العناصر بدرجات أكسدة مختلفة في المركبات التي يتكون منها الطلاء، يعطي الطلاء مدى واسعًا جدًا من الألوان المختلفة والجذابة [12].
كيمياء أحمر الشفاه
متداول استخدامه كثيرًا لدى السيدات أما عن تركبيه الكيميائي فالكثير يجهل، مم يتكون؟!

مادة اللانولين، بي واكس وزيت الخروع إضافة إلى زيوت وشموع أخرى.
تقريبًا هذه هي الكميات الوسطية لتركيبة أحمر الشفاه وقد يكون هناك اختلافات قليلة بالنسب بحسب النوعية.
الزيوت والشموع المضافة لأحمر الشفاه:
يقوم الشمع بإعطاء أحمر الشفاه شكله وقوامه ويستخدم أعداد كبيرة ومتنوعة من الشمع في صناعته ويعتمد اختيار المادة الشمعية المناسبة بحسب درجة ذوبانها بحيث تكون مقاومة لدرجات الحرارة العالية نسبيًا، كما أنه مطرى أثناء الاستخدام ليمنع جفاف الشفاه.
أما عن الزيوت فتستخدم للترطيب ويستخدم بشكل كبير زيت الزيتون بالإضافة لزيوت صناعية أخرى.
أما بالنسبة للأصبغة والألوان:
تتنوع الأصبغة المستخدمة بشكل هائل، لإعطاء كمية واسعة من الألوان فأحمر الشفاه يتكون من مادة الايوزين Eosin التي تتفاعل مع الأحماض الأمينية المتواجدة في بروتينات الجلد في الشفاه فتعطي لونًا أحمر وتشتق هذه المادة بشكل رئيسي من الحشرات.

مادة الـEosin المتواجدة في أحمر الشفاه عند تفاعله مع الأحماض الأمينية في الجلد يتحول لذلك المركب الذي يعطي اللون الأحمر القرمزي carmine red
مكونات أخرى في أحمر الشفاه:
توضع العديد من المكونات مثل المواد المخففة للتهيج ومواد لتحسين الطعم [13].
كيمياء مواد التنظيف
- من حسن الحظ أن الكيمياء موجودة لمساعدتنا في العديد من الأمور اليومية مثل إزالة البقع.
يمكن تصنيف البقع إلى عدة أنواع بحسب الجزيئات التي تتكون منها: إنزيمية، أو أكسيدية، أو دهنية، أو جسيمات. لكن في الواقع قد يكون لبقعة أكثر من مكون ونوع، مثلًا بقعة صلصة الباستا لها مكون مؤكسد ومن المحتمل أيضًا أن تكون دهنية قليلًا. على هذا النحو، تميل مزيلات البقع إلى أن تكون خليطًا من جميع العوامل التي سنناقشها، لمعالجة هذه البقع متعددة المكونات.
النوع الأول : البقع الإنزيمية
تشمل البقع الإنزيمية بقع الدم وبقع الحشائش، والتي هي إلى حد كبير نتيجة للبروتينات. يمكن استخدام الإنزيمات في تركيبات مزيلات البقع لكسر هذا النوع. على وجه التحديد، سوف يقوم البروتياز (Protease) بتكسير البروتينات عن طريق كسر الجزيئات الأكبر إلى قطع أصغر قابلة للذوبان. يمكن أيضًا إزالة بقع العرق البشري عن طريق البروتياز.

جزيء بروتين يكسر بواسطة Protease إلى أجزاء صغيرة وأحماض أمينية
النوع الثاني: البقع المؤكسدة
غالبًا ما تقع البقع الملونة الزاهية في فئة البقع المؤكسدة. وتشمل هذه البقع الشاي والقهوة، في هذه الحالة استخدام مزيل البقع المبني على التبييض قد يكون مفيدًا. فتحتوي مزيلات البقع هذه على عوامل تبييض، عادةً بيروكسيد الهيدروجين H2O2، الذي يكسر الأجزاء المسببة للون من الهياكل الكيميائية، ويزيل مظهر البقعة. بيروكسيد الهيدروجين موجود عادة في شكل بيكربونات الصوديوم، الذي يطلق بيروكسيد الهيدروجين عندما يقترن بالماء. لكن هناك مشكلة صغيرة حيث إن بيروكسيد الهدروجين لا يعمل فوق الدرجة 40 مئوية لذلك يجب إضافة (tetraacetylethylenediamine (TAED. يتفاعل TAED مع بيروكسيد الهيدروجين لإنتاج حمض البيركتيك، وهو عامل تبييض أقوى من بيروكسيد الهيدروجين.
النوع الثالث: البقع الشحمية الزيتية
في حين أن الزيوت والشحوم يمكن تقسيمها بواسطة إنزيمات الليبيز (Lipase هو انزيم يقوم بتكسير الدهون من جزيئات كبيرة إلى جزيئات أصغر لتسهيل إزالته من الملابس)، فإنها تتم إزالتها في المقام الأول عن طريق استخدام خافضات التوتر السطحي.
تقوم هذه المواد الخافضة للتوتر السطحي بإزالة الزيوت والشحوم من خلال تشكيل هياكل تسمى “micelles” عبارة عن تجمعات كروية صغيرة تحتوي في داخلها الزيت ومن خارجها الماء، بنفس طريقة عمل الصابون في إزالة الزيوت والشحوم، انظر للصورة أدناه. تتحلل الأجزاء القابلة للذوبان في الزيت وتذوب فيها، لتشكل بنية كروية حول قطرة الزيت. ثم تلتصق الأجزاء القابلة للذوبان في الماء من جزيء التفاعل بالسطح للخارج، وهذا يعني أن المذيبات قادرة على الذوبان في الماء، مما يسمح بلف البقعة الدهنية.
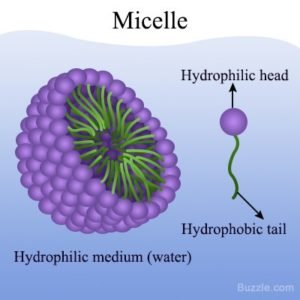
الجزيئات المستخدمة في إزالة البقع الدهنية تشبه الجزيئات الموجودة في الغشاء البلازمي للخلية حيث تتكون من ذيل كاره للماء ورأس محب للماء، فعند وضع هذه الجزيئات مع ماء على البقع الدهنية فستلتصق البقع الدهنية بالذيل الكاره للماء ويحبس داخل الكرة بينما الرأس المحب للماء سوف يكون مقابلًا للماء ويذوب فيه وهكذا دواليك حتى يتم حبس كل جزيئات الزيت داخل هذه الكرات وتنظف قطعة الملابس.
محب للماء: Hydrophilic
كاره للماء: Hydrophobic
النوع الرابع: البقع الجسيمية
بالنسبة للبقع الجسيمية، يتم استخدام المركبات المشار إليها باسم “builders”. تساعد هذه المركبات في المقام الأول على تلطيف المياه أثناء الغسل عن طريق إزالة أيونات المعادن الإيجابية (خاصة أيونات الكالسيوم والمغنيسيوم) من الماء. كما أنها مفيدة للغاية في إزالة بقع التربة من الملابس، لأن هذه البقع غالبًا ما تكون مرتبطة بالأقمشة بواسطة حاجز من أيونات الكالسيوم. لذا إزالة أيونات الكالسيوم يساعد على إزالة الأوساخ [14].
إعلان
